Cientistas descobriram um mecanismo genético que pode indicar novas maneiras de tratar uma infecção fúngica rara, mas mortal, que levou várias unidades de terapia intensiva a fechar. A descoberta traz uma esperança inicial contra um patógeno que tem sido difícil de controlar e praticamente impossível de tratar após a sua disseminação.
Candida auris é especialmente perigoso para pessoas já gravemente enfermas, deixando os hospitais altamente vulneráveis a surtos. Embora o fungo possa existir na pele sem causar sintomas, pacientes que dependem de ventiladores estão em um risco muito maior. Com a infecção, cerca de 45% dos pacientes morrem, e o fungo é resistente a todos os principais tipos de medicamentos antifúngicos. Essa resistência torna o tratamento extremamente desafiador e consente que o patógeno persista nos leitos hospitalares.
Uma ameaça global à saúde com origens misteriosas
A infecção foi detectada pela primeira vez em 2008, e sua origem ainda é desconhecida. Desde então, surtos foram relatados em mais de 40 países, incluindo o Reino Unido. Candida auris, também conhecida como Candidozyma auris, é agora reconhecida como uma grave ameaça à saúde global e aparece na lista de patógenos fúngicos de prioridade crítica da Organização Mundial da Saúde. No Reino Unido, o número de casos reportados continua a aumentar de forma constante.
Investigando a infecção em um modelo vivo
Pesquisadores da Universidade de Exeter deram um importante passo à frente ao examinar como os genes são ativados durante a infecção por Candida auris. Esta é a primeira vez que tal atividade genética foi estudada em um hospedeiro vivo usando um modelo baseado em larvas de peixe. O estudo foi publicado na revista Communications Biology da editora Nature e contou com o apoio da Wellcome, do Conselho de Pesquisa Médica (MRC) e do Centro Nacional de Substituição, Redução e Refinamento (NC3Rs).
Os pesquisadores afirmam que os resultados podem ajudar a identificar um alvo biológico para novos tratamentos antifúngicos ou até mesmo permitir a reutilização de medicamentos já existentes, se o mesmo comportamento genético for confirmado durante a infecção em humanos.
O projeto foi co-liderado pelo Professor Clínico NIHR Hugh Gifford do Centro de Micoses Médicas (CMM) da Universidade de Exeter. Ele disse: “Desde que surgiu, Candida auris causou estragos onde se instala nas unidades de terapia intensiva hospitalares. Pode ser fatal para pacientes vulneráveis, e os hospitais gastaram milhões na difícil missão de erradicação. Acreditamos que nossa pesquisa pode ter revelado um ponto fraco neste patógeno letal durante a infecção ativa, e precisamos urgentemente de mais estudos para explorar se conseguimos encontrar medicamentos que visem e explorem essa fraqueza.”
Por que os modelos de pesquisa tradicionais foram insuficientes
Um dos maiores desafios ao estudar Candida auris tem sido sua capacidade de sobreviver a altas temperaturas. Quando combinado com sua resistência incomum ao sal, isso levou alguns pesquisadores a sugerir que ele pode ter se originado em oceanos tropicais ou animais marinhos. Essas características também dificultaram seu estudo utilizando modelos laboratoriais convencionais.
Para superar isso, a equipe de Exeter desenvolveu um novo modelo de infecção utilizando peixes killifish árabes. Os ovos dessa espécie podem sobreviver a temperaturas semelhantes às do corpo humano, tornando-os adequados para observar infecções em condições que se assemelham à doença real.
Atividade genética revela possíveis vulnerabilidades
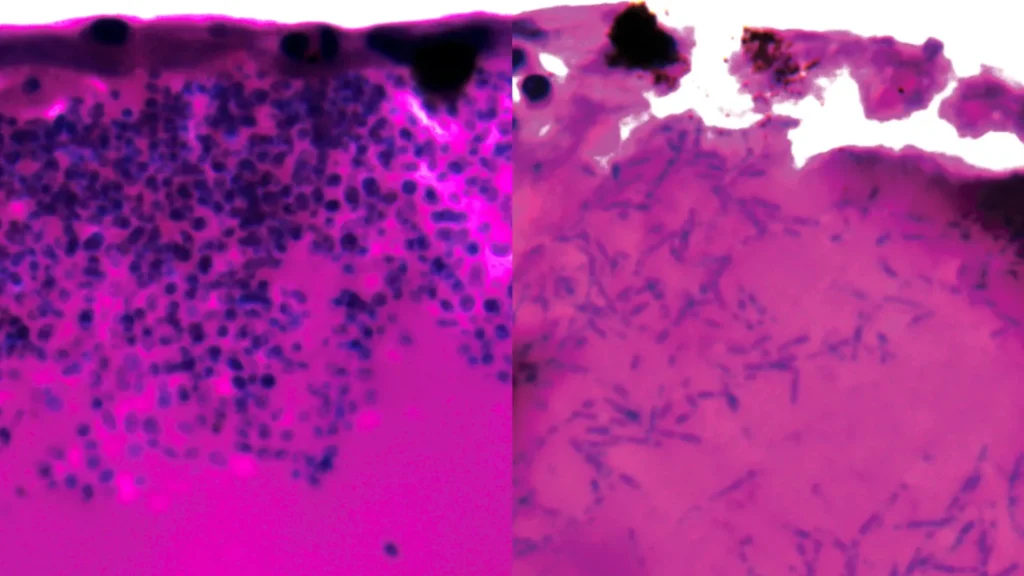
Durante os experimentos, os pesquisadores observaram que Candida auris pode alterar sua forma formando estruturas fúngicas alongadas conhecidas como filamentos. Essas estruturas podem ajudar o fungo a buscar nutrientes enquanto infecta um hospedeiro.
A equipe também analisou quais genes estavam ativos ou desativados durante a infecção para identificar possíveis pontos fracos. Vários dos genes que se tornaram ativos são responsáveis por produzir bombas de nutrientes que capturam moléculas que escaneiam ferro e transportam ferro para as células fúngicas. Como o ferro é essencial para a sobrevivência, esse processo pode representar uma vulnerabilidade crítica.
O co-autor sênior Dr. Rhys Farrer, do Centro de Micoses Médicas da Universidade de Exeter, disse: “Até agora, não sabíamos quais genes estão ativos durante a infecção em um hospedeiro vivo. Agora precisamos descobrir se isso também ocorre durante a infecção em humanos. O fato de termos encontrado genes ativados para capturar ferro fornece pistas sobre onde Candida auris pode se originar, como um ambiente marinho com pouco ferro. Isso também nos dá um alvo potencial para novos medicamentos e aqueles que já existem.”
Esperança para tratamentos futuros
Dr. Gifford, que também atua como médico residente em terapia intensiva e medicina respiratória no Royal Devon & Exeter Hospital, enfatizou a importância clínica das descobertas. Ele disse: “Embora ainda haja várias etapas de pesquisa a serem realizadas, nossa descoberta pode ser uma perspectiva emocionante para um tratamento futuro. Temos medicamentos que visam as atividades de captura de ferro. Agora precisamos explorar se eles podem ser reaproveitados para impedir que Candida auris mate humanos e feche unidades de terapia intensiva hospitalares.”
O modelo de larvas de killifish árabes foi desenvolvido com apoio de uma bolsa de projeto do NC3Rs como uma alternativa ao uso de modelos de camundongos e zebrafish, que são comumente utilizados para estudar interações entre patógenos e seus hospedeiros. A Dra. Katie Bates, chefe de financiamento de pesquisa do NC3Rs, afirmou: “Esta nova publicação demonstra a utilidade do modelo alternativo para estudar a infecção por Candida auris e permitir visões sem precedentes sobre eventos celulares e moleculares em hospedeiros infectados vivos. Este é um brilhante exemplo de como abordagens inovadoras alternativas podem superar limitações-chave dos estudos tradicionais com animais.”
O artigo se intitula ‘Expressão de genes transportadores de xenosideróforos e filamentação específica de clado na infecção por Candida auris em killifish (Aphanius dispar)’ e foi publicado na revista Communications Biology da editora Nature.