Os pesquisadores também integraram ferramentas de Inteligência Artificial, incluindo aprendizado de máquina, para analisar padrões de biomarcadores. Esses métodos possibilitaram a diferenciação precisa entre pacientes com Long COVID e indivíduos saudáveis, além de identificar as combinações de biomarcadores mais informativas. Tais descobertas podem apoiar diagnósticos mais exatos e tratamentos personalizados no futuro.
O que são armadilhas extracelulares de neutrófilos (NETs)?
Dr. Alain Thierry e sua equipe no Instituto de Câncer de Montpellier (IRCM) da INSERM, em Montpellier, foram alguns dos primeiros a ressaltar a importância dos NETs na COVID-19. Os NETs se formam quando os neutrófilos liberam seu DNA por meio de um processo chamado NETose, criando estruturas filamentosas repletas de enzimas nocivas que podem rapidamente aprisionar e neutralizar micro-organismos invasores.
Embora os NETs ajudem a defender contra infecções, a produção excessiva deles pode ser prejudicial. A formação excessiva de NETs está ligada a condições inflamatórias e de coagulação graves, incluindo infecções severas, doenças autoimunes, câncer, diabetes e artrite. Dr. Thierry observa que a produção contínua de NETs, impulsionada por ciclos de inflamação e formação de coágulos, pode agravar a gravidade da doença.
Diante disso, as equipes lideradas pela Prof. Pretorius e pelo Dr. Thierry colaboraram para investigar se microcoágulos e NETs interagem em pacientes com Long COVID.
Descobertas principais
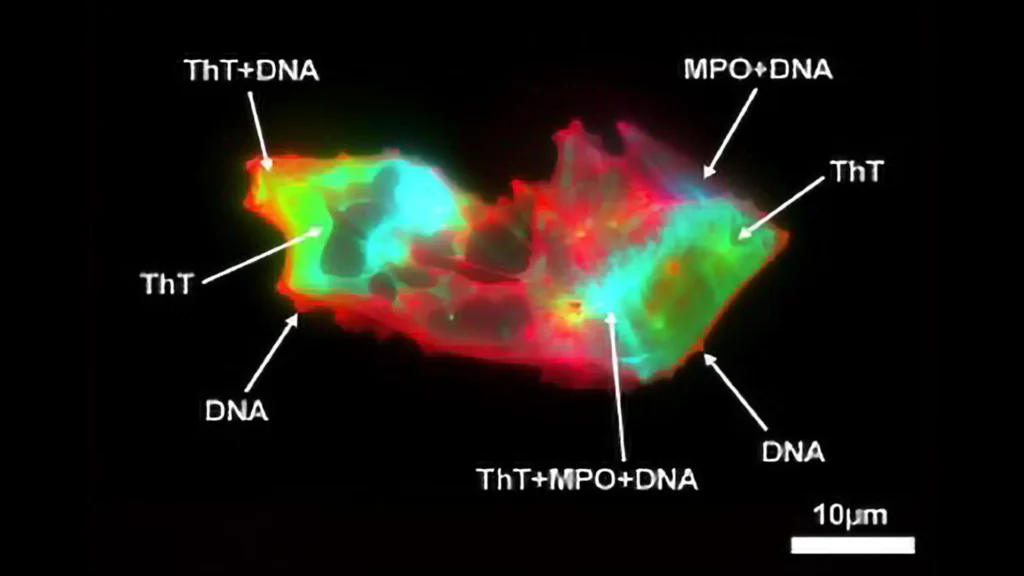
Usando citometria de fluxo de imagem e microscopia de fluorescência, os pesquisadores realizaram medições detalhadas de microcoágulos e NETs no plasma de indivíduos com Long COVID e compararam os resultados com controles saudáveis. Eles também quantificaram os NETs por meio da avaliação de marcadores proteicos e DNA circulante.
Relataram várias observações significativas:
- Os biomarcadores associados tanto a microcoágulos quanto a NETs estavam significativamente elevados em pacientes com Long COVID.
- Os pacientes mostraram não apenas um aumento no número de microcoágulos, mas também microcoágulos maiores.
- O mais notável foi que a equipe identificou uma relação estrutural entre microcoágulos e NETs. Essa associação apareceu em todas as amostras, mas foi muito mais substancial em pessoas com Long COVID.
“Essa descoberta sugere a existência de interações fisiológicas subjacentes entre microcoágulos e NETs que, quando desreguladas, podem se tornar patogênicas,” explica Dr. Thierry.
Os pesquisadores também integraram ferramentas de Inteligência Artificial, incluindo aprendizado de máquina, para analisar padrões de biomarcadores. Esses métodos possibilitaram a diferenciação precisa entre pacientes com Long COVID e indivíduos saudáveis, além de identificar as combinações de biomarcadores mais informativas. Tais descobertas podem apoiar diagnósticos mais exatos e tratamentos personalizados no futuro.
A Prof. Pretorius enfatiza que o estudo revela um acúmulo de microcoágulos no plasma de pacientes com Long COVID, provavelmente favorecido pela atividade excessiva de NETs: “Essa interação pode tornar os microcoágulos mais resistentes à fibrinólise, promovendo sua persistência na circulação e contribuindo para complicações microvasculares crônicas,” ela explica.
Ao esclarecer como os NETs podem estabilizar os microcoágulos, o estudo fornece informações valiosas sobre os processos biológicos envolvidos no Long COVID. As descobertas também destacam possíveis abordagens terapêuticas voltadas à redução da coagulação prejudicial e da inflamação.
Além disso, o trabalho avança na busca por novos biomarcadores que possam ajudar a diagnosticar e gerenciar o Long COVID. Como os autores observam, “A combinação de técnicas de imagem avançadas e aprendizado de máquina confere robustez metodológica e contribui significativamente para o discurso científico em andamento sobre síndromes pós-virais.”
Em pacientes com Long COVID, um novo estudo revelou uma associação estrutural entre microcoágulos circulantes e armadilhas extracelulares de neutrófilos (NETs).
Essa descoberta sugere a existência de interações fisiológicas subjacentes entre microcoágulos e NETs que, quando desreguladas, podem se tornar patogênicas.
O que são microcoágulos?
O termo microcoágulos, recentemente adotado na literatura científica, refere-se a agrupamentos anormais de proteínas de coagulação sanguínea que circulam na corrente sanguínea do paciente. O conceito foi introduzido em 2021 pela Prof. Resia Pretorius do Departamento de Ciências Fisiológicas da Universidade de Stellenbosch, quando descobriram a presença anormal desses microcoágulos nas amostras de sangue de pacientes com COVID-19. Essa descoberta gerou ampla atenção durante a pandemia devido ao seu potencial papel nas coagulopatias relacionadas ao COVID.
O que são armadilhas extracelulares de neutrófilos (NETs)?
A equipe do Dr. Alain Thierry no Instituto de Câncer de Montpellier (IRCM) da INSERM, em Montpellier, esteve entre os primeiros a identificar o papel crítico dos NETs na patogênese da COVID-19. Os NETs são produzidos por meio de uma forma especializada de resposta imune inata conhecida como NETose, onde os neutrófilos expelirem seu DNA para formar estruturas filamentosas carregadas de enzimas citotóxicas capazes de rapidamente aprisionar e neutralizar patógenos.
No entanto, a formação excessiva de NETs pode se tornar prejudicial, contribuindo para uma ampla gama de doenças inflamatórias e trombóticas, incluindo infecções severas, distúrbios autoimunes, câncer, diabetes e artrite.
Segundo Dr. Thierry, a produção persistente de NETs, alimentada por ciclos autoperpetuantes de inflamação e trombose, pode agravar a gravidade da doença.
Em um esforço colaborativo, as equipes da Prof. Pretorius e do Dr. Thierry investigaram a possível interação entre microcoágulos e NETs no contexto do Long COVID.
Descobertas principais
Utilizando citometria de fluxo de imagem e microscopia de fluorescência, realizaram uma análise quantitativa e estrutural de microcoágulos e NETs no plasma de pacientes com Long COVID, comparando com controles saudáveis. Os NETs também foram quantificados através da análise de marcadores proteicos e DNA circulante.
- Observou-se um aumento significativo em biomarcadores associados a microcoágulos e NETs nas amostras dos pacientes.
- Microcoágulos estavam não só mais presentes, mas também maiores em tamanho entre os pacientes.
- Mais importante, descobriram uma associação estrutural anteriormente não relatada entre microcoágulos e NETs, observada em todos os sujeitos, mas muito mais pronunciada em pacientes com Long COVID.
“Essa descoberta sugere a existência de interações fisiológicas subjacentes entre microcoágulos e NETs que, quando desreguladas, podem se tornar patogênicas,” explica Dr. Thierry.
Além disso, a integração de ferramentas de Inteligência Artificial, como aprendizado de máquina, na análise de biomarcadores possibilitou distinguir pacientes com Long COVID de indivíduos saudáveis com alta precisão. Os algoritmos identificaram as combinações de biomarcadores mais preditivas, melhorando a confiabilidade diagnóstica e abrindo caminho para abordagens de medicina personalizada.
Segundo a Prof. Pretorius, os resultados revelam um acúmulo significativo de microcoágulos no plasma de pacientes com Long COVID, provavelmente impulsionado e estabilizado pela produção excessiva de NETs: “Essa interação pode tornar os microcoágulos mais resistentes à fibrinólise, promovendo sua persistência na circulação e contribuindo para complicações microvasculares crônicas,” ela explica.
Ao identificar o papel mecanicista dos NETs na estabilização de microcoágulos, este estudo fornece novos insights sobre a fisiologia do Long COVID. Essas descobertas apoiam o desenvolvimento de estratégias terapêuticas direcionadas à modulação das respostas trombo-inflamatórias.
Finalmente, o estudo abre caminho para a elaboração de biomarcadores inovadores para diagnóstico e gerenciamento: “A combinação de técnicas de imagem avançadas e aprendizado de máquina confere robustez metodológica e contribui significativamente para o discurso científico em andamento sobre síndromes pós-virais,” concluem.