O transtorno depressivo maior (TDM) é um problema de saúde global significativo e uma das principais causas de incapacidade. Aproximadamente 30% das pessoas diagnosticadas com depressão desenvolvem depressão resistente ao tratamento (DRT), o que significa que seus sintomas não melhoram de forma satisfatória com os medicamentos antidepressivos padrão. O cetamina tem atraído atenção como um antidepressivo de ação rápida para pessoas com DRT. No entanto, os cientistas ainda não compreendem completamente como ele funciona no cérebro humano, o que dificulta o refinamento e a personalização desse tratamento.
Um novo estudo publicado na Molecular Psychiatry em 5 de março de 2026, buscou esclarecer esse mistério. A pesquisa foi liderada pelo Professor Takuya Takahashi, do Departamento de Fisiologia da Escola de Medicina da Universidade da Cidade de Yokohama, no Japão. A equipe utilizou um método avançado de tomografia por emissão de pósitrons (PET) para observar diretamente as mudanças no receptor de glutamato α-amino-3-hidroxi-5-metil-4-isoxazole propanoico (AMPAR). Este receptor é uma proteína chave que ajuda a regular a comunicação entre as células do cérebro e desempenha um papel importante na plasticidade sináptica e na sinalização glutamatérgica em pacientes que recebem cetamina.
O Prof. Takahashi explicou: “Embora a cetamina tenha demonstrado efeitos antidepressivos rápidos em pacientes com depressão resistente ao tratamento, seu mecanismo molecular no cérebro humano ainda não estava claro.”
Visualizando Receptores Cerebrais com um Novo Traçador PET
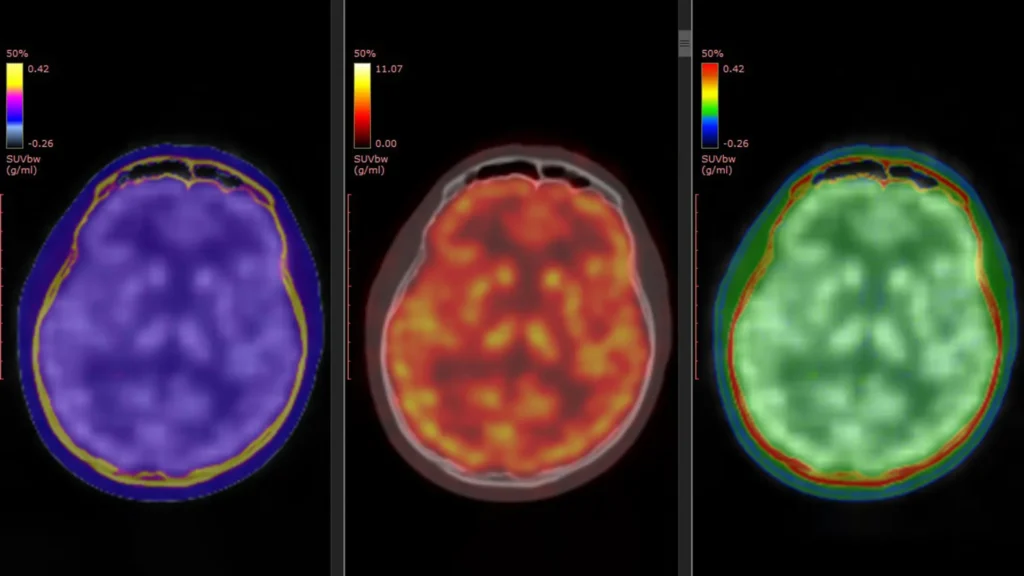
A pesquisa contou com um traçador PET desenvolvido anteriormente pela equipe, conhecido como [¹¹C]K-2. Este traçador permite que os cientistas visualizem diretamente os AMPAR na superfície celular no cérebro humano vivo. Estudos laboratoriais e em animais anteriores sugeriram que os efeitos antidepressivos da cetamina envolvem atividade de AMPAR. A nova pesquisa fornece as primeiras evidências diretas desse processo ocorrendo em humanos.
Para realizar o estudo, os pesquisadores combinaram dados de três ensaios clínicos registrados realizados no Japão. O grupo de estudo incluiu 34 pacientes diagnosticados com DRT e 49 participantes saudáveis que serviram como controles.
Os pacientes receberam cetamina intravenosa ou um placebo durante um período de duas semanas. A imagem cerebral PET foi realizada antes do início do tratamento e novamente após a infusão final. Essa abordagem permitiu aos pesquisadores comparar as mudanças nos níveis de AMPAR e a distribuição no cérebro ao longo do tempo.
Mudanças Cerebrais Específicas de Região Ligadas ao Alívio dos Sintomas
Os resultados mostraram que pessoas com DRT apresentavam anomalias generalizadas na densidade de AMPAR em comparação com os participantes saudáveis. Essas diferenças apareceram em regiões específicas do cérebro, em vez de em todo o cérebro como um todo.
A cetamina não produziu mudanças uniformes em todo o cérebro. Em vez disso, as melhorias nos sintomas depressivos estavam ligadas a ajustes dinâmicos e específicos da região nos níveis de AMPAR. Algumas áreas corticais mostraram aumento na densidade dos receptores, enquanto reduções foram observadas em regiões associadas ao processamento de recompensas, especialmente a habenula. Essas mudanças específicas de região estavam fortemente conectadas a melhorias nos sintomas depressivos dos pacientes.
“O efeito antidepressivo da cetamina em pacientes com DRT é mediado por mudanças dinâmicas no AMPAR no cérebro humano vivo,” explicou o Prof. Takahashi. “Usando um novo traçador PET, [11C]K-2, conseguimos visualizar como a cetamina altera a distribuição de AMPAR em regiões específicas do cérebro e como essas mudanças se correlacionam com as melhorias nos sintomas depressivos.”
Essas observações fornecem evidências humanas diretas que apoiam mecanismos previamente identificados em estudos com animais e os conectam a efeitos clínicos antidepressivos reais.
Potencial Marcador Bioquímico para Prever Resposta ao Tratamento
As descobertas não apenas esclarecem como a cetamina funciona, mas também podem ter um valor clínico prático. A imagem PET de AMPAR poderia potencialmente servir como um marcador que ajuda os médicos a avaliar e prever como indivíduos com DRT responderão ao tratamento com cetamina.
Como muitos pacientes não respondem a antidepressivos padrão, a identificação de marcadores biológicos confiáveis para a resposta ao tratamento continua sendo um objetivo importante nos cuidados de saúde mental.
Rumo a Tratamentos Mais Personalizados para a Depressão
Ao permitir que os cientistas observem diretamente a atividade de AMPAR no cérebro humano vivo, esta pesquisa ajuda a preencher uma lacuna de longa data entre a pesquisa laboratorial e a psiquiatria clínica. Os resultados identificam a modulação de AMPAR como um mecanismo central por trás dos efeitos antidepressivos rápidos da cetamina e sugerem que a imagem PET de AMPAR poderia orientar estratégias de tratamento mais personalizadas no futuro.
Em última análise, esse trabalho pode apoiar o desenvolvimento de terapias mais precisas para pessoas que sofrem de depressão resistente ao tratamento.
Este trabalho foi apoiado pelo Ministério da Educação, Cultura, Esportes, Ciência e Tecnologia (Fundos de Coordenação Especiais para Promoção da Ciência e Tecnologia); pela Agência de Pesquisa e Desenvolvimento Médico do Japão (AMED) (números de concessão: JP18dm0207023, JP19dm0207072, JP24wm0625304, JP25gm7010019 e JP20dm0107124); pela Sociedade Japonesa para Promoção da Ciência KAKENHI (números de concessão: 22H03001, 20H00549, 20H05922, 23K10432, 19H03587, 20K20603, 22K15793 e 21K07508); pela Fundação Takeda de Ciência; pelo Programa do Projeto de Pesquisa de Próxima Geração da Keio; pela Fundação de Pesquisa Médica SENSHIN; e pela Fundação de Pesquisa Clínica do Japão.